pero ¿que es un indicador químico?
Un indicador químico es un ácido o base débil cuya forma tiene diferente color que la forma sin combinar , esto es debido a que están formados por sistemas resonantes aromáticos, que pueden modificar la distribución de carga según la forma que adopten. Esta alteración por el desplazamiento hacia una forma mas o menos disociada, hace que la absorción energética del sistema se modifique y con ello el color.
en otras palabra un indicadores químicos son sustancias que permiten una transformacional notoria en el producto final.
Tenemos distintos tipos:
Indicadores ácido-base o de neutralización
Es una reacción entre un ácido y una base que se llama neutralización. Cuando en la reacción participa un ácido fuerte y una base fuerte se obtiene una sal y agua. Se puede decir que la neutralización es la combinación de iones hidronio y de aniones de hidróxido para formar moléculas de agua. Durante este proceso se forma una sal.
cambian de color dentro un pequeño intervalo de PH. cada indicador tiene su intervalo muy característico y por lo general cambia de color al añadir una base a un ácido.
Las reacciones de neutralización son generalmente exotérmicas, lo que significa que desprenden energía en forma de calor.
Podemos resumir el proceso así:
ácido + base → sal + agua
Indicadores oxidación-reducción
Un indicador redox (oxidación reducción) es una sustancia cuyo color es intenso, bien definido, y distinto en sus estados oxidado y reducido. Estas sustancias requieren sólo un ligero cambio en la proporción de un estado u otro, para variar de color, ya que el color se puede apreciar aún cuando la concentración del indicador es baja. Entonces, cuando se ha llegado al punto de equivalencia, una sola gota más del tinte hará variar al indicador.
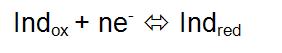
Indicadores de precipitación
Indica cuando una reacción de precipitación a finalizado. se forma un precipitado que contiene la coloración de la sustancia.
Las coloraciones:
indicadores químicos comunes
Bibliográfia
Anon, (2017). [online] Available at: http://www.heurema.com/QG/QG7/INDICADORESAB1.pdf [Accessed 19 Oct. 2017].
Anon, (2017). [online] Available at: http://recursostic.educacion.es/newton/web/materiales_didacticos/acidosbases/reacacidobase.html [Accessed 19 Oct. 2017].
2.bp.blogspot.com. (2017). Citar un sitio web - Cite This For Me. [online] Available at: https://blogger.googleusercontent.com/img/b/R29vZ2xl/AVvXsEj-Tnb_HQ_5ut_7rQSLUtfHH0VFAwQklBn9wIqppJdHP0NN9Q4Nz7mpYM7pbkYrCYcZmhsHH473unuLbH7XikYoby17ocgPfk68wv5dm4ENsy4qlQEU9FkMndyriPMY0mApks8BcpeiNQ01/s1600/erlenmeyer+chulos+coloridos+quimica+xuxte.jpg [Accessed 19 Oct. 2017].
Quimica.laguia2000.com. (2017). Indicador redox | La Guía de Química. [online] Available at: https://quimica.laguia2000.com/conceptos-basicos/indicador-redox [Accessed 19 Oct. 2017].Quimitube.com. (2017). Mecanismo de los indicadores ácido base e intervalo de viraje | Quimitube. [online] Available at: http://www.quimitube.com/videos/teoria-8-indicadores-acido-base [Accessed 19 Oct. 2017].




